 Como registrar DIU na ANVISA?
Como registrar DIU na ANVISA?
Você quer saber como registrar DIU na ANVISA? Neste conteúdo vamos te explicar tudo sobre este método utilizado pelas mulheres e também sobre os passos para ser feito o registro.
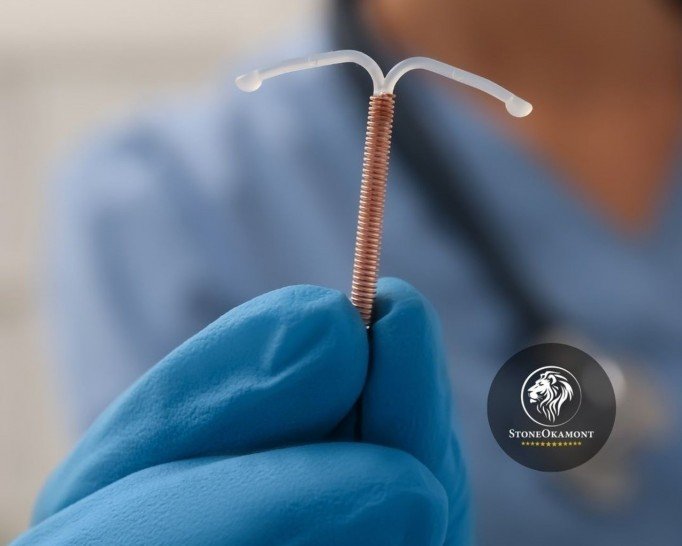
O Dispositivo Intrauterino (DIU) é uma pequena estrutura em formato de T, inserida dentro do útero da mulher e trata-se de um método é utilizado para prevenir a gravidez, ele pode ser constituído por cobre, hormônios entre outras combinações, possuindo diversas vantagens e desvantagens, apesar de serem utilizados com o mesmo objetivo.
Para registrar DIU na ANVISA, existem várias instruções normativas, regras e etapas que devem ser seguidas junto à ANVISA. Lidar com a burocracia é complicado, entre em contato com a Stone Okamont, nós fazemos todo o trabalho para você do início ao fim. Sem retrabalhos e gastos desnecessários.
Veja quais são os passos necessários para registrar DIU na ANVISA.
Tópicos deste blog
1º passo: Licença de Funcionamento
Antes de registrar DIU na ANVISA, o primeiro passo é obter a Licença de Funcionamento para seu estabelecimento. Ela é adquirida a partir de uma vistoria realizada pela VISA, ou seja, a Vigilância Sanitária Local.
A Stone Okamont atua com excelência na elaboração do processo de Licença de Funcionamento junto à VISA.
A Licença de Funcionamento é um documento de aprovação junto a Vigilância Sanitária local, reconhecendo que seu estabelecimento possui condições técnicas e operacionais para realizar sua atividade e te levar para o próximo passo que é a Autorização de Funcionamento Empresa.
2º passo: Autorização de Funcionamento Empresa
A Autorização de Funcionamento de Empresa, mais conhecida como AFE é um documento emitido pela ANVISA, publicado no Diário Oficial da União (DOU), o mesmo te habilita a exercer sua atividade na qual foi peticionada junto à Agência. A obtenção da AFE, significa que a empresa atua de acordo com a legislação brasileira e está apta para atuar em todo território nacional, para registrar Imunoglobulina na ANVISA.
A Autorização de Funcionamento de Empresa é necessária e indispensável para o próximo passo que é o peticionamento do CBPF, ou seja, certificado de Boas Práticas de Fabricação.
3 º passo: Preciso do Certificado de Boas Práticas de Fabricação para registrar DIU na ANVISA?
O Certificado de Boas Práticas de Fabricação (CBPF), é o documento que atesta o cumprimento das diretrizes da legislação vigente para a fabricação de um determinado produto. É emitido para comprovar que a empresa foi instruída e inspecionada durante o processo de fabricação.
Antes de registrar DIU na ANVISA, primeiro é preciso classificá-lo.
A ANVISA classifica o DIU como classe de risco IV, ou seja, segundo as legislações vigentes, produtos de classe de risco III e IV precisam obrigatoriamente do Certificado de Boas Práticas junto à ANVISA é uma exigência da ANVISA, que tem um dos parâmetros mais aprimorados do mundo, atestando que o estabelecimento cumpre com as Boas Práticas de Fabricação.
4° passo: Registro de DIU na ANVISA
O Registro de Produto é o documento emitido pela ANVISA legalizando a comercialização do mesmo. A partir desse momento, para registrar DIU na ANVISA, a agência irá analisar a petição da maneira mais adequada, verificando a documentação apresentada para certificar que a empresa está de acordo com a legislação vigente e apta a desenvolver suas atividades.
Nessa etapa final do registro do DIU são apresentadas informações do produto como: material de composição, instruções de uso, instruções de descarte entre outros. Dessa maneira, deve-se respeitar o processo de peticionamento, devendo-se anexar a documentação obrigatória e protocolar a petição na ANVISA.
Todas as empresas que ofereçam produtos que possam ser prejudiciais à saúde, como medicamentos, agrotóxicos, cosméticos, etc; necessitam estar em dia com todas as regularizações junto à ANVISA.
Etapas concluídas, você já pode registrar DIU na ANVISA!
Os processos burocráticos para regularizar uma empresa e obter o Registro de DIU não são nada fáceis. Para isso a Stone Okamont oferece a você um serviço de qualidade dispondo de excelentes profissionais que farão da burocracia um alívio no seu tempo que sabemos quão precioso é.
Entre em contato conosco! Preencha o formulário abaixo, fale com um de nossos profissionais e tire todas as suas dúvidas sobre como registrar DIU na ANVISA.
Quer saber qual o caminho ideal
PARA A SUA EMPRESA?
Solicite aqui um orçamento.


